El intestino, el órgano inmune más grande del cuerpo
La estructura intestinal es crucial para la salud y el rendimiento de los animales. Además de las funciones digestivas del tracto gastrointestinal (TGI), las células inmunes y las estructuras linfoides presentes en el TGI constituyen el órgano inmune más grande del cuerpo.
Las bases del sistema inmune asociadas a la mucosa intestinal se dividen en cinco esferas, que son:
Barrera epitelial, barrera física, capa celular epitelial (enterocitos y colonocitos), células caliciformes productoras de moco (células caliciformes), células de Paneth productoras de sustancias bactericidas (defensinas), células portadoras (células M), linfocitos T intraepiteliales (Figura 1);
Folículos linfoides aislados, sitio de inicio de las respuestas inmunes adaptativas, estructura organizada de las poblaciones de células inmunes;
Placas de Peyer, sitio de inicio de las respuestas inmunes adaptativas, estructura organizada de varios folículos linfoides con centros germinales;
Tejido linfoide difuso, macrófagos, células dendríticas, mastocitos, linfocitos T irritantes, células T reguladoras, plasmocitos secretores de IgA dispersos en la propia lámina de la mucosa y;
Ganglios linfáticos mesentéricos, sitio de inicio de las respuestas inmunes adaptativas contra los antígenos intestinales traídos por el sistema linfático (Gonçalves et al., 2016).
Figura 1. Estructura de defensa de la barrera epitelial intestinal (adaptado de D. Artis. 2008; 8:411 Nature Reviews Immunology).
Superfície intestinal
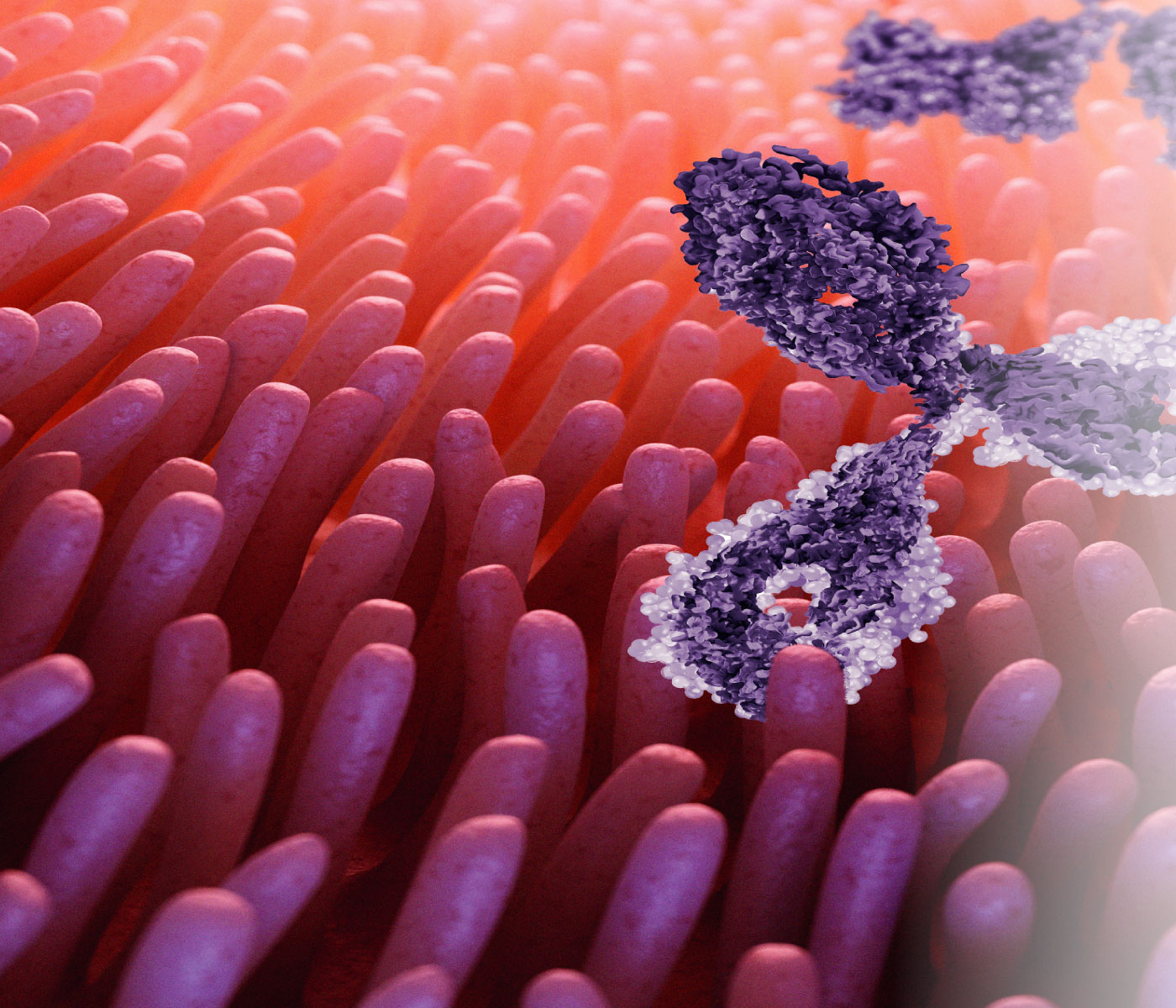
La superficie de la mucosa (Figura 2) está recubierta con un moco formado por mucinas, que son secretadas por las células caliciformes y crean una barrera que evita que las partículas más grandes, incluida la mayoría de las bacterias, entren en contacto directo con la capa de células epiteliales (Turner, 2009).
Las mucinas contienen diferentes oligosacáridos e incluyen glicoproteínas secretadas y de la superficie celular. Las mucinas secretadas, incluyendo MUC2, MUC5 y MUC6, forman un gel hidratado de 300 a 700 μm de espesor que tiene dos capas: una capa externa menos densa que normalmente está colonizada por bacterias y una capa interna densa que está unida al epitelio y está libre de bacterias.
Figura 2. Representación del epitelio de la mucosa intestinal.
Las células de Paneth (Figura 3), ubicadas en las criptas del intestino delgado, secretan α-defensina. Mientras que en el colon, los tallos de β-...