O problema das micotoxinas em grãos e concentrados para ruminantes
Os fungos toxigênicos utilizam como substrato alimentos de uso animal e humano, e produzem micotoxinas, metabólitos secundários de baixo peso molecular e alta toxicidade (Zain, 2011). Particularmente, grãos e concentrados de origem vegetal são os substratos ideais para o seu crescimento (Yiannikouris e Jouany, 2002). A colonização dos grãos por fungos pode ocorrer antes da colheita ou posteriormente, durante o armazenamento.
 As micotoxinas, por sua vez, podem ser produzidas tanto na fase de crescimento exponencial do fungo quanto durante a fase estacionária, e representam um importante risco à saúde animal e humana (Bullerman e Draughon, 1994). Em humanos, a intoxicação pode ocorrer pelo consumo de alimentos contaminados de origem vegetal e também pela ingestão de alimentos de animais que, por sua vez, consumiram alimentos contaminados (OMS, 2018).
As micotoxinas, por sua vez, podem ser produzidas tanto na fase de crescimento exponencial do fungo quanto durante a fase estacionária, e representam um importante risco à saúde animal e humana (Bullerman e Draughon, 1994). Em humanos, a intoxicação pode ocorrer pelo consumo de alimentos contaminados de origem vegetal e também pela ingestão de alimentos de animais que, por sua vez, consumiram alimentos contaminados (OMS, 2018).
EFEITOS NOS RUMINANTES
![]() Em geral, os animais estão expostos à intoxicação por micotoxinas devido ao tipo de alimento que consomem, seja grãos ou concentrados. Os ruminantes são mais resistentes aos efeitos tóxicos produzidos pelas micotoxinas em comparação aos animais monogástricos, e essa maior resistência seria devida à ação da microbiota ruminal que degrada e inativa esses metabólitos (Fink-Gremmels, 2008). Mesmo assim, são descritos inúmeros efeitos tóxicos associados ao consumo de alimentos com micotoxinas.
Em geral, os animais estão expostos à intoxicação por micotoxinas devido ao tipo de alimento que consomem, seja grãos ou concentrados. Os ruminantes são mais resistentes aos efeitos tóxicos produzidos pelas micotoxinas em comparação aos animais monogástricos, e essa maior resistência seria devida à ação da microbiota ruminal que degrada e inativa esses metabólitos (Fink-Gremmels, 2008). Mesmo assim, são descritos inúmeros efeitos tóxicos associados ao consumo de alimentos com micotoxinas.
Os principais gêneros toxicogênicos que contaminam grãos destinados a ruminantes são Fusarium, Aspergillus e Penicillium (Bonifaz, 2012).
Os fungos do gênero Fusarium são amplamente difundidos e geralmente contaminam a cultura ao se desenvolverem antes do armazenamento. Principalmente as culturas de trigo, cevada e milho são contaminadas com estes fungos quando as condições de umidade e temperatura são favoráveis.

O problema das micotoxinas em grãos e concentrados para ruminantes
Além das perdas agrícolas, diversas espécies produzem micotoxinas que causam intoxicações tanto em ruminantes quanto em humanos e outros animais (Zinedine et al., 2007). As principais toxinas produzidas por este gênero de fungos são as fumonisinas, os tricotecenos e a zearalenona.
• As fumonisinas causam efeitos toxicológicos importantes, uma vez que interferem no metabolismo dos esfingolípidos (Marasas, 1995) e o mais importante, a fumonisina B1, tem sido associada ao aparecimento de cancro do esôfago em humanos (EFSA, 2005). A Agência Internacional de Pesquisa sobre o Câncer (IARC) considera-o um possível carcinógeno humano (grupo 2B).
![]() Em animais, têm sido mais estudados em suínos e equinos. Os ruminantes – especialmente o gado de corte – parecem ser mais resistentes à sua toxicidade. No entanto, sabe-se que as fumonisinas são pouco metabolizadas no rúmen, têm efeitos hepato e nefrotóxicos e têm um impacto negativo no consumo e na produção em vacas leiteiras (Smith, 2012).
Em animais, têm sido mais estudados em suínos e equinos. Os ruminantes – especialmente o gado de corte – parecem ser mais resistentes à sua toxicidade. No entanto, sabe-se que as fumonisinas são pouco metabolizadas no rúmen, têm efeitos hepato e nefrotóxicos e têm um impacto negativo no consumo e na produção em vacas leiteiras (Smith, 2012).
• Os tricotecenos, o desoxinivalenol (DON) e a toxina T-2, por outro lado, são metabolizados no rúmen em um metabólito muito menos tóxico, portanto dificilmente causam alterações em ruminantes (Eriksen e Pettersson, 2004), embora os autores anteriores destaquem a informação limitada que existe a este respeito.
• A zearalenona possui configuração molecular tridimensional semelhante ao estradiol, por isso pode ocupar seus receptores, estimulando-os e atuando então como desregulador endócrino em machos e fêmeas de diferentes espécies animais (D’Mello et al., 1999, Haschek et al., 2002).
![]() Nas fêmeas bovinas promovem impacto negativo na fertilidade, produzindo estro anormal, vaginite, redução da sobrevivência embrionária e fetal, vulvovaginite e prolapso retal. Sofre desintoxicação ao nível do rúmen, embora em vacas leiteiras que consomem dietas com elevados níveis de contaminação, a zearalenona e seus derivados tenham sido detectados no leite (Liu y Applegate, 2020).
Nas fêmeas bovinas promovem impacto negativo na fertilidade, produzindo estro anormal, vaginite, redução da sobrevivência embrionária e fetal, vulvovaginite e prolapso retal. Sofre desintoxicação ao nível do rúmen, embora em vacas leiteiras que consomem dietas com elevados níveis de contaminação, a zearalenona e seus derivados tenham sido detectados no leite (Liu y Applegate, 2020).
 Nos machos, observa-se uma síndrome de feminização e diminuição dos níveis de testosterona, peso testicular, espermatogênese e libido (Zinedine et al, 2007).
Nos machos, observa-se uma síndrome de feminização e diminuição dos níveis de testosterona, peso testicular, espermatogênese e libido (Zinedine et al, 2007).
Enquanto isso, fungos das espécies dos gêneros Aspergillus e Penicillium desenvolvem-se principalmente durante o armazenamento. Os Aspergillus são reconhecidos pela sua capacidade de produzir toxinas potentes, como aflatoxinas e ocratoxinas (Navale et al., 2021).
• As aflatoxinas são hepatotóxicas, imunossupressoras, mutagênicas, teratogênicas e carcinogênicas em todas as espécies, incluindo humanos (Zain, 2011), sendo uma delas, a aflatoxina B1, o agente carcinogênico natural mais potente conhecido (Coppock et al., 2018).
![]() Os efeitos também podem ser agudos ou crônicos, dependendo da dose e do tempo de exposição. Principalmente em vacas e outros ruminantes leiteiros, a intoxicação crônica tem grande relevância para a saúde pública, uma vez que tanto a aflatoxina B1 quanto seu metabólito M1 (que é eliminado no leite) são carcinogênicos para humanos (IARC, 1993; IARC, 2002), bem como um imunossupressor para bezerros lactentes.
Os efeitos também podem ser agudos ou crônicos, dependendo da dose e do tempo de exposição. Principalmente em vacas e outros ruminantes leiteiros, a intoxicação crônica tem grande relevância para a saúde pública, uma vez que tanto a aflatoxina B1 quanto seu metabólito M1 (que é eliminado no leite) são carcinogênicos para humanos (IARC, 1993; IARC, 2002), bem como um imunossupressor para bezerros lactentes.
• Por sua vez, as ocratoxinas, nefrotóxicas e imunossupressoras, também são produzidas por diversas espécies de fungos do gênero Penicillium (Perrone e Susca, 2017). A ocratoxina A é extremamente potente, mas os efeitos negativos em ruminantes são raros, uma vez que é transformada no rúmen em compostos menos ativos por protozoários (Mobashar et al., 2010).
O problema das micotoxinas em grãos e concentrados para ruminantes
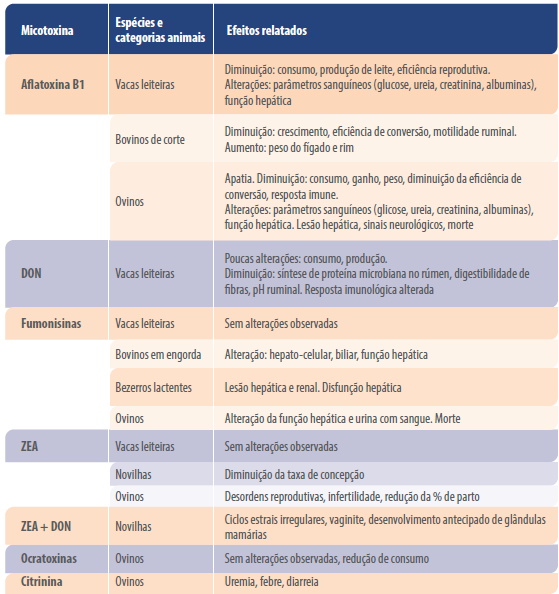
A Tabela 1 resume os principais efeitos observados pelo consumo de micotoxinas em ruminantes, relatados por Gallo et al. (2015) num trabalho de revisão, confirmando que a informação é relativamente escassa e pouco conclusiva, aspecto que os autores destacam.
Tabela 1. Principais efeitos das micotoxinas em ruminantes observados em trabalho experimental ou de campo (resumido de Gallo et al., 2015).
O problema das micotoxinas em grãos e concentrados para ruminantes
![]() Além de ações específicas em tecidos ou órgãos, as micotoxinas raramente produzem intoxicação aguda e os sintomas em ruminantes são geralmente bastante inespecíficos. A diminuição da produção ou consumo sem causa aparente, a rejeição de alimentos, a maior susceptibilidade a doenças, falhas reprodutivas ou abortos podem ser causadas pela presença de micotoxinas nos alimentos, embora esta presença muitas vezes passe despercebida se o diagnóstico não for feito de forma adequada.
Além de ações específicas em tecidos ou órgãos, as micotoxinas raramente produzem intoxicação aguda e os sintomas em ruminantes são geralmente bastante inespecíficos. A diminuição da produção ou consumo sem causa aparente, a rejeição de alimentos, a maior susceptibilidade a doenças, falhas reprodutivas ou abortos podem ser causadas pela presença de micotoxinas nos alimentos, embora esta presença muitas vezes passe despercebida se o diagnóstico não for feito de forma adequada.
INÍCIO DA CONTAMINAÇÃO E CONDIÇÕES DE DESENVOLVIMENTO
![]() O crescimento dos fungos e a produção de toxinas não são constantes, mas dependem das condições ambientais como umidade e temperatura. Em geral, condições de alta temperatura e umidade ambiental favorecem tanto o crescimento do fungo quanto a produção de micotoxinas.
O crescimento dos fungos e a produção de toxinas não são constantes, mas dependem das condições ambientais como umidade e temperatura. Em geral, condições de alta temperatura e umidade ambiental favorecem tanto o crescimento do fungo quanto a produção de micotoxinas.
Os fungos podem crescer nos alimentos sem necessariamente produzir micotoxinas, mas quando confrontados com certos fatores de estresse, sintetizam-nas. Assim, condições climáticas extremas de seca ou umidade, presença de grãos danificados, ou mau manejo da colheita ou armazenamento, são fatores que desencadeiam o estresse e com ele a produção de micotoxinas (Whitlow e Hagler, 2005).
Neste sentido, os fenômenos relacionados com as alterações climáticas parecem estar a modificar os padrões de apresentação dos surtos de micotoxicoses, que estão a surgir em regiões onde antes não ocorriam (Tolosa et al., 2021).
 A contaminação fúngica nos grãos (e portanto a concentração de micotoxinas) não é uniforme, sendo comum que, em lotes, silos ou outros locais de armazenamento, apareçam setores mais contaminados que outros, como “focos de acumulação” (Food Safety authority of Ireland, 2009) e até mesmo que existem diferenças entre grãos do mesmo lote (Tittlemier et al., 2022).
A contaminação fúngica nos grãos (e portanto a concentração de micotoxinas) não é uniforme, sendo comum que, em lotes, silos ou outros locais de armazenamento, apareçam setores mais contaminados que outros, como “focos de acumulação” (Food Safety authority of Ireland, 2009) e até mesmo que existem diferenças entre grãos do mesmo lote (Tittlemier et al., 2022).
É importante levar em consideração essas variações na amostragem de grãos para detecção de micotoxinas: durante a amostragem deve-se seguir um protocolo específico para o tipo de material e armazenamento, extraindo material de diversas áreas, levando em consideração as diferentes profundidades e alturas.
 Em silos de grãos de sorgo úmido armazenados em sacos, García e Santos et al. (2020) relatam um efeito benéfico do tempo de armazenamento. Se o armazenamento ocorrer em condições adequadas, o baixo pH sustentado ao longo do tempo reduz a concentração de taninos condensados (que no grão são potenciais protetores contra a contaminação fúngica, mas dificultam a fermentação ruminal) e reduz a contaminação fúngica.
Em silos de grãos de sorgo úmido armazenados em sacos, García e Santos et al. (2020) relatam um efeito benéfico do tempo de armazenamento. Se o armazenamento ocorrer em condições adequadas, o baixo pH sustentado ao longo do tempo reduz a concentração de taninos condensados (que no grão são potenciais protetores contra a contaminação fúngica, mas dificultam a fermentação ruminal) e reduz a contaminação fúngica.
Segundo este trabalho, 180 dias de armazenamento em sacos seriam ideais para melhorar a fermentação ruminal de grãos de difícil digestão e reduzir a contaminação. Segundo García e Santos et al. (2022), em silos de grãos de sorgo a abundância relativa de Fusarium diminuiu após 30 dias de armazenamento, e em grãos com alto teor de tanino Aspergillus spp diminuiu.
• Essas descobertas abrem uma nova perspectiva sobre possíveis vantagens da utilização de grãos com alto teor de taninos para a confecção de silagens, pelo menos em ambientes com alto risco de contaminação por fungos.
Uma característica das micotoxinas é a sua resistência aos tratamentos de processamento de alimentos. Resistem à secagem, à trituração e são muito estáveis termicamente, pelo que a cozedura dificilmente os elimina (Kabak, 2009). Tudo isso dificulta muito o seu controle, e os nutricionistas sabem que quando se trata de controlar as micotoxinas, “tudo é pouco” em termos de prevenção.
![]() É neste sentido que se recomenda para alimentos: a identificação e quantificação de fungos toxicogênicos e a determinação e quantificação de concentrações de micotoxinas. Com essas informações, podem ser tomadas medidas de controle e prevenção para mitigar o risco de contaminação em alimentos para consumo humano e animal.
É neste sentido que se recomenda para alimentos: a identificação e quantificação de fungos toxicogênicos e a determinação e quantificação de concentrações de micotoxinas. Com essas informações, podem ser tomadas medidas de controle e prevenção para mitigar o risco de contaminação em alimentos para consumo humano e animal.
IDENTIFICAÇÃO E QUANTIFICAÇÃO
Para a identificação e quantificação de fungos toxicogênicos contaminantes de alimentos, o isolamento e a identificação morfológica são historicamente realizados de acordo com suas características fenotípicas. Nestes métodos, as colônias desenvolvidas a partir de culturas alimentares isoladas são contadas e transferidas para meios específicos para identificação ao microscópio óptico pelas suas características micro e macromorfológicas de acordo com as chaves de identificação convencionais correspondentes para os principais gêneros de fungos.
Esses métodos são muito trabalhosos, exigem muita experiência e treinamento e também consomem muito tempo. Atualmente, existem métodos moleculares baseados em PCR para identificação e quantificação, que evitam os problemas levantados acima.
Esses métodos permitem a identificação de isolados em nível de espécie através de amplificação e sequenciamento de diferentes genes (Ward et al., 2002; O’Donnell et al., 2004) ou por amplificação com primers específicos (Nicolaisen et al., 2009; Scauflaire et al., 2012).
Para determinar e quantificar as concentrações de micotoxinas nos alimentos, diferentes métodos imunoensaios e cromatográficos podem ser realizados (Díaz e Smith, 2005). Técnicas cromatográficas como cromatografia em camada delgada (TLC), cromatografia líquida (HPLC), cromatografia líquida de ultra-desempenho (UHPLC) e cromatografia líquida – espectrometria de massa (LC-MS).

Este último método LC-MS está sendo amplamente desenvolvido, devido ao seu grande potencial para avaliar grandes quantidades de amostras e diferentes micotoxinas simultaneamente (Krska et al., 2008). Outra metodologia utilizada atualmente é uma técnica imunocromatográfica rápida combinada e integrada.

Este método combina anticorpos numa única tira de membrana, permitindo assim a detecção de vários analitos em apenas alguns minutos. Requer equipamento portátil de cromatografia de fluxo lateral, que permite determinar concentrações de uma ampla gama de micotoxinas nos próprios estabelecimentos.
CONTROLE + PREVENÇÃO
 Para controlar e prevenir a contaminação por fungos toxicogênicos e micotoxinas nos alimentos, o manejo deve começar no campo, o que inclui o tipo de semeadura, variedade de cultura, controle de ervas daninhas, irrigação e rotação de culturas (Edwards, 2004). Como os fatores climáticos não podem ser controlados e influenciam o desenvolvimento de fungos e micotoxinas, as medidas utilizadas no campo muitas vezes não são eficientes e devem ser tomadas medidas durante a colheita e o armazenamento.
Para controlar e prevenir a contaminação por fungos toxicogênicos e micotoxinas nos alimentos, o manejo deve começar no campo, o que inclui o tipo de semeadura, variedade de cultura, controle de ervas daninhas, irrigação e rotação de culturas (Edwards, 2004). Como os fatores climáticos não podem ser controlados e influenciam o desenvolvimento de fungos e micotoxinas, as medidas utilizadas no campo muitas vezes não são eficientes e devem ser tomadas medidas durante a colheita e o armazenamento.
Durante a colheita devem ser evitados danos ao grão, pois o predispõe à contaminação por fungos e micotoxinas. Já no armazenamento, pode ser possível controlar a umidade e a temperatura para que o risco de contaminação possa ser reduzido (Shapira & Paster, 2004). Ambiente ácido e baixa atividade de água são formas eficazes de controlar e inibir o crescimento bacteriano. No entanto, os fungos podem crescer sob uma gama mais ampla de condições físico-químicas do que a maioria das bactérias.
Nos produtos alimentícios, os fungos proliferam em faixas de pH entre 2 e 9, com atividades de água de 0,61 a 0,99 (Snyder et al., 2019). Também no armazenamento podem ser utilizadas substâncias que inibem o crescimento de fungos, mas estas não atuam no conteúdo de micotoxinas caso estas já existam.
Quando os alimentos são contaminados por micotoxinas, uma das estratégias utilizadas para controlá-los é a aplicação de agentes sequestrantes. Estas substâncias são polímeros inorgânicos ou orgânicos de alto peso molecular que reduzem a absorção de micotoxinas no trato digestivo, diminuindo sua toxicidade no organismo animal.
Para isso, os sequestrantes formam complexos irreversíveis com essas toxinas na luz intestinal e são posteriormente eliminados nas fezes (Devegowda e Murthy, 2005). A maioria são compostos orgânicos, inorgânicos ou multimodulares (Díaz e Smith, 2005).
🔒 Conteúdo exclusivo para usuários registrados.
Cadastre-se gratuitamente para acessar esta publicação e muito mais conteúdo especializado. Leva apenas um minuto e você terá acesso imediato.
Conecte-seRegistre-se em nutriNews
REGISTRE-SE
















